干細胞治療94例肝衰竭的臨床應用案例發表時間:2021-01-22 16:29作者:杭吉干細胞科技 干細胞(MSCS)在特定誘導條件下可分化為脂肪、骨、軟骨、肌肉、韌帶、神經、肝、心肌、內皮等多種組織和細胞。 且具有向多種組織分化潛能和強大自我再生能力,并可在體外誘導下分化為具有肝細胞活性類的肝細胞,為肝衰竭患者治療提供了新的途徑。 肝衰竭是由多種因素導致肝臟合成、解毒、排泄和生物轉化等功能發生嚴重障礙或失代償而引起的一種嚴重肝損傷,病死率極高。在我國,引起肝衰竭的首要病因是乙型肝炎病毒(HBV)感染,HBV相關慢加急性肝衰竭(HBV—ACLF)主要是病毒誘發的機體免疫病理性損傷所引起。
肝衰竭傳統干預方法無法滿足患者需求臨床治療多采用綜合療法,近年來,部分醫院 開展了“人工肝”支持療法,但難以從根本上阻止和 逆轉肝壞死。雖然血漿透析濾過(plasma dialysis fil. tration,PDF)和肝移植術可挽救部分患者的生命,但 也存在術后并發癥、免疫排斥和肝源供體緊缺等問 題。 干細胞給治療肝衰竭帶來新方向近年來。以干細胞為基礎的細胞治療應用于臨床各領域,其中骨髓干細胞是一類能在體外分化、增殖的低免疫原性成體干細胞,具有自我更新、多向分化潛能
干細胞治療肝衰竭的三種機制1、干細胞具有很強的趨化性和再生能力的 既往研究證實,將動員后的骨髓干細胞移植到患者肝臟內,能分化為肝樣細胞。并進一步代替損傷的肝細胞, 促進肝細胞再生。從而促進肝臟功能的恢復。 2、歸巢效應 在肝內移植后,干細胞可直接到達受損的肝損傷部位,一方面可分化成新的肝臟功能細胞,增加肝細胞數量,或還能“催醒”自身肝臟細胞。 另有體外細胞遷移實驗表明,經轉染而高表達干細胞其遷移能力(歸巢性)顯著升高,肝細胞生長因子(HGF)參與其中。 3、旁分泌與免疫調節 干細胞不僅分泌多種免疫調節因子,還可抑制轉化分泌肝細胞生長因子(hepatocyte growth factor,HGF)、IL1、IL6等促炎癥因子釋放促進組織再生、抗纖維化作用。 干細胞通過分泌細胞因子(SDF-1α)激活卵圓細胞、促進肝細胞再生作用 。抑制了免疫反應和炎癥反應,促進的肝臟組織器官的修復和內源性肝臟干細胞的增殖,促進肝細胞的再生,從而達到了治療效果 臨床研究目的:探討采取自體骨髓干細胞移植治療慢加急性乙型肝炎肝衰竭(HBV—ACLF)患者的療效。 方法:科研團隊在青海某院肝腎內科就診的94例HBV—ACLF患者.被隨機分為對照組47例和觀察組47例,在內科綜合治療的基礎上分別給予血漿透析濾過(PDF)和PDF聯合經肝動脈自體骨髓干細胞移植治療。采用美國東部腫瘤協作組評分(ECOG)和終末期肝病模型(MELD)評分評價生活質量和肝功能狀態。 結果:兩組生存患者肝功能變化的比較在治療24周末,觀察組生存患者血清ALB水平顯著高于對照組(P<0.05,表1)。
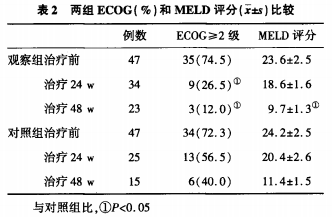
兩組ECOG和MELD評分比較在治療24周和 48周時。觀察組ECOG評級I>2級發生率顯著低于 對照組(P<0.05);在治療48周時,觀察組生存患者 MELD評分顯著低于對照組(P<0.05,表2)。說明加用干細胞移植治療可進一步改善患者的健康狀況。
綜上所述干細胞療法以其獨特類肝細胞多向分化潛力、歸巢性、旁分泌和免疫調節特性等優勢有望成為治療肝衰竭新途徑。 但肯定的是干細胞移植聯合PDF治療有效的改善慢加急性肝衰竭患者肝功能,促進蛋白合成,緩解病情,提高生存率和生活質量。 隨著大量臨床轉化實驗開展及對干細胞療法特性認識不斷深入,其將為肝衰竭干預提供更多支持與幫助,造福所有患者。 |
行業動態 干細胞治療 干細胞移植 |