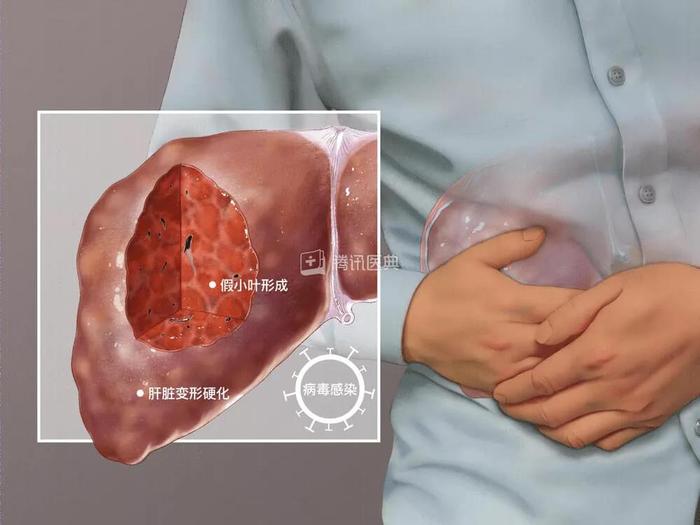
干細胞療法治療肝硬化的主要機制原理是什么發表時間:2021-02-25 15:40作者:杭吉干細胞科技 干細胞在醫學上被稱為“通用細胞”。由于其具有多向分化潛能、低免疫原性和免疫調節功能,在免疫調節、減輕炎癥反應和損傷修復等方面有著廣闊的應用前景。近年來,干細胞移植干預肝硬化的研究較多,傳統的干預方法效果不佳,干細胞移植在這方面表現出很大的潛力。 一、引起肝硬化的原因 引起肝硬化的原因很多,在國內以乙型病毒性肝炎所致的肝硬化最為常見,少部分為酒精性肝硬化和血吸蟲性肝硬化。在國外,特別是北美、西歐則以酒精中毒最多見。 1、病毒性肝炎:乙型、丙型和丁型肝炎病毒引起的慢性肝炎是我國肝硬化的主要病因,占50~60%。病毒持續存在、中到重度的肝臟壞死炎癥以及纖維化是演變為肝硬化的主要原因。 2、慢性酒精性肝病是歐美國家肝硬化最常見的原因。 3、非酒精性脂肪性肝病是僅次于上述兩種病因的最為常見的肝硬化前期病變,且有增加趨勢。 4、長期的膽汁淤積、藥物或毒物、遺傳和代謝性疾病、血吸蟲病、免疫紊亂等均可造成肝細胞變性、壞死、纖維化,進而進展為肝硬化。 5、誘發因素:肝硬化由多種慢性肝病進展而來,因此,任何對肝臟正常功能有影響的不良因素,均可視作肝硬化的誘發因素,如嗜酒、肥胖、糖尿病、高甘油三脂血癥、過度勞累、化學藥物、某些保健品等。
傳統方法干預肝硬化效果不理想 中國被認為是肝病的大國,據2018年統計,全球各類肝病患者超過13億人,中國超過3.93億人,約占全球肝病患者的30%。世界衛生組織估計,到2030年,中國將有超過1億人衰亡于慢性肝病。然而,目前臨床對肝硬化的干預情況并不理想,缺乏有效的干預藥物和方法治療肝功能不足。目前,常規有效的干預方法是肝移植,但由于合適的肝臟來源有限,不能滿足臨床需要。目前迫切需要發展一種新的肝硬化的干預方法。 干細胞療法為治療肝硬化提供了一種新途徑 間充質干細胞具有獨特的免疫調節作用、自我更新和跨胚胎多向分化潛能。目前,科學家發現,干細胞除了具有多向分化潛能外,還能在肝臟受損時通過旁分泌分泌一系列生長因子、細胞因子等信號分子。 這些因素不僅能調節免疫功能,減少炎癥反應,抗肝細胞凋亡,促進血管增生,抗肝纖維化等損傷肝組織的修復,還能促進干細胞的多向分化,動員卵細胞。卵細胞進入受損肝臟,促進內源性肝干細胞的分化,刺激內源性肝細胞的增殖,為干細胞移植干預肝病提供了新的方向。
干細胞療法治療肝硬化的五種機制 1、干細胞具有獨特的免疫表型,可以低表達MHC-I分子,不表達MHC-Ⅱ類分子、FasL和T細胞共刺激分子B7,因此其免疫原性很弱。在合適的體外分化條件下,干細胞可以在內胚層向肝實質細胞分化,干細胞也可以分化為內胚層肝實質細胞,且移植后無排斥反應。干細胞還能分泌可溶性細胞因子介導免疫抑制,誘導免疫耐受,抑制免疫細胞向肝臟的增殖和遷移,減輕受損肝臟的免疫炎癥,提高肝病患者的生存率。 2、干細胞可分泌相關細胞因子,如基質細胞衍生因子1(SDF-1)、血管內皮生長因子(Vii GF)、IGF.1等,通過旁分泌機制抑制各種類型受體細胞的凋亡,其中SDF-1/CXCR-4軸起重要調節作用。 3、干細胞移植可減少肝組織膠原沉積,抑制肝細胞轉化生長因子-β1和平滑肌肌動蛋白的表達,降低肝纖維化程度。 4、干細胞在不同細胞因子的作用下可分化為不同的細胞類型。當肝損傷的局部微環境發生改變時,可產生多種炎癥信號分子,促進和促進干細胞的分化,而HGF、FGFs、TGF-β、表皮生長因子、IL-IO等因子的反應性分泌可促進受損肝組織的修復。 5、因干細胞具有多向分化潛能,干細胞可分化為內胚層肝細胞、膽管細胞和血管內皮細胞,從而為新生血管及其側支的形成提供營養支持。
臨床案例:北京某醫院感染科于2020年對16例肝硬化患者進行了干細胞移植的臨床研究。隨訪18個月后,10例患者的初始膽紅素水平在6個月以上得到改善,6例移植后12個月后略有升高,表明干細胞移植的效果明顯。 綜上所述:干細胞療法主要通過干細胞的旁分泌作用如抗凋亡、抗炎、抗纖維化、刺激內源性細胞的分化、增殖和新生血管等途徑治療肝病。許多臨床研究表明,干細胞移植在肝臟疾病的介入治療中有很強的臨床應用價值。 |
行業動態 干細胞治療 干細胞移植 |