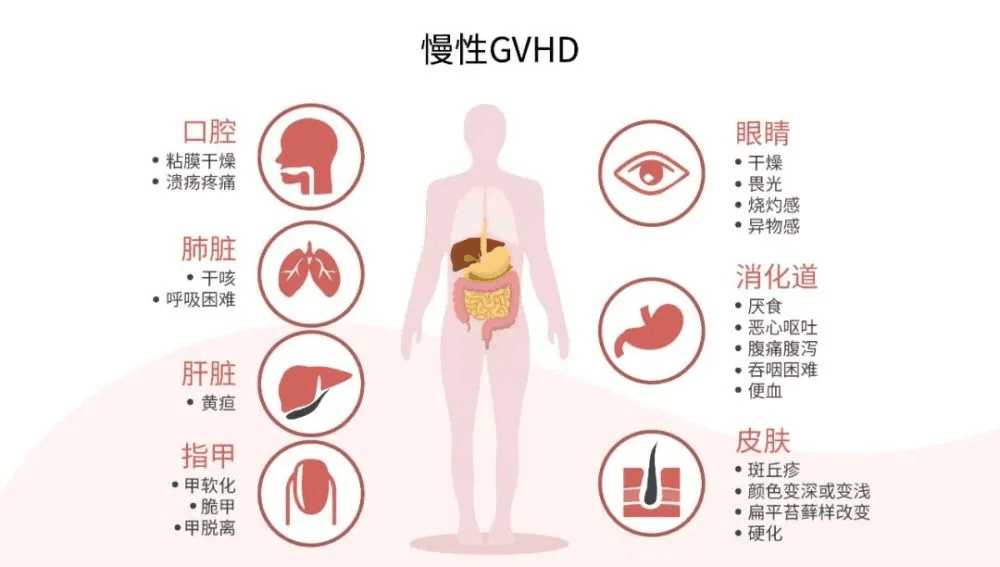
間充質干細胞療法治療移植物抗宿主病的臨床試驗現狀發表時間:2022-06-13 18:57 移植物抗宿主病 (GVHD) 是造血干細胞移植后(HSCT) 常見的致命并發癥,其中類固醇被用作治療選擇。然而,目前還沒有針對產生類固醇抵抗 (SR) 的患者的二線治療。間充質干細胞(MSCs)具有免疫調節功能,可對炎癥微環境發揮免疫抑制作用。 大量體外實驗證實,間充質干細胞可以顯著抑制先天性和適應性免疫細胞的增殖或活化。在移植物抗宿主病小鼠模型中,MSCs改善了體重減輕并提高了存活率。因此,MSCs用于預防或治療移植物抗宿主病的臨床轉化前景廣闊,迄今為止已經進行了多項臨床試驗。 介紹慢性移植物抗宿主病(cGVHD)指異基因造血干細胞移植后,受者在重建供者免疫的過程中,來源于供者的淋巴細胞攻擊受者臟器產生的臨床病理綜合征,通俗來講即“免疫排異反應”引起的疾病。
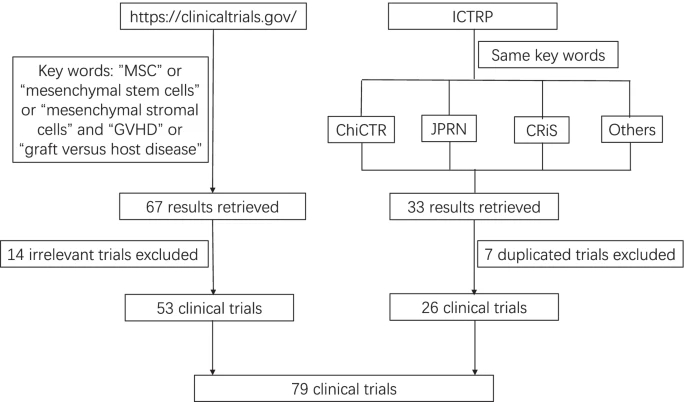
造血干細胞移植 (HSCT) 是常規治療無法治愈的血液疾病患者的最佳治療方式。HSCT手術量逐年增加,根據國際血液和骨髓移植研究中心(CIBMTR)的統計,2019年美國進行的手術超過22,000例,其中自體HSCT超過14,000例,自體HSCT超過8000例。 同年,我國完成異基因HSCT近萬例。在HSCT期間,移植的免疫活性淋巴細胞可以廣泛識別受體抗原。這些免疫反應在促炎微環境中發展,導致 GVHD 的臨床表現,包括皮疹、血清膽紅素水平升高和腹瀉。在對HLA相同的兄弟姐妹進行的HSCT中,急性 GVHD (aGVHD) 發生率約為40%,對于 HLA 不匹配的無關供體,達到 80%。 急性GVHD根據其表現的嚴重程度分為四類:I(輕度)、II(中度)、III(嚴重)和IV(非常嚴重)。此外,35-50% 接受HSCT的患者發展為慢性 GVHD (cGVHD)。在控制 GVHD 的嘗試中,各種免疫抑制劑已被用于GVHD的臨床預防和治療。類固醇方案仍然是標準治療,有效性低于 50%,目前沒有標準的二線治療。嚴重 GVHD 患者的總生存率很低,III 級為 25%,IV級為 5% 。GVHD 對患者的生存構成越來越大的威脅。因此,需要新的有效治療方法。 間充質干細胞為什么能治療移植物抗宿主病? 間充質干細胞是一類具有自我更新和多項分化潛能的多能干細胞,主要來源于臍帶、胎盤、牙髓、脂肪、骨髓等組織中,具有低免疫原性、多項分化潛能、造血支持和獨特的免疫調節等特點。 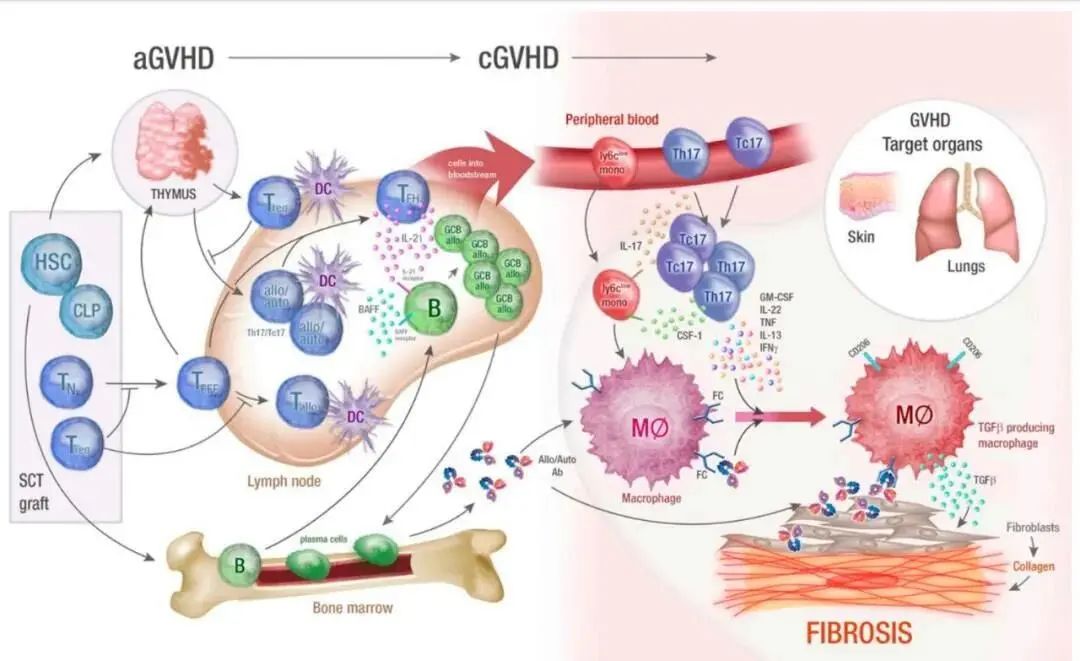 間充質干細胞的作用機制是在炎癥環境調控下發揮的免疫調節功能和其強大的旁分泌作用。此外它還有組織修復功能,如對肺、消化道粘膜、過關節病變、神經損傷等有一定修復作用。 干細胞移植移植物抗宿主病臨床試驗概述為了全面分析間充質干細胞療法預防或治療移植物抗宿主病的臨床試驗,我們檢索關鍵詞“MSCs”或“間充質干細胞”或“間充質基質細胞”和“GVHD”或“移植物抗宿主病”。臨床試驗.gov并獲得了67個結果。在分析每個檢索到的結果后,排除了14個不相關的臨床試驗。 接下來,我們搜索了世界衛生組織的國際臨床試驗注冊平臺國際臨床試驗注冊平臺(ICTRP)搜索門戶,鏈接到不同國家的臨床試驗注冊平臺。使用與上述相同的關鍵字,我們檢索了每個列出的國家或地區的臨床試驗注冊平臺,不包括已在http://clinicaltrials.gov上注冊的7個試驗,并發現了額外的26項試驗(中國臨床試驗注冊中心 (ChiCTR) 上的7項試驗、日本初級注冊網絡 (JPRN) 上的5項試驗、韓國臨床研究信息服務 (CRiS) 上的1項試驗、伊朗臨床試驗注冊中心的1項試驗) IRCT),歐盟臨床試驗注冊中心9個,澳大利亞新西蘭臨床試驗注冊中心 (ANZCTR)3個)。 因此,選擇了79項臨床試驗(圖 1),共招募了4710名受試者。我們對所有檢索到的臨床試驗進行了編號(附加文件1:表S1),當下面再次提到臨床試驗時,我們將使用其編號而不是其完整的NCT或ID編號。除臨床試驗No.50和No.51為擴大訪問研究類型和試驗No.57為觀察性研究類型外,其余均為介入性試驗。除了12號試驗在包括一名男性患者后終止,其他臨床試驗包括男性和女性患者。我們分析了79項臨床試驗的研究設計、階段、地點和其他特征。
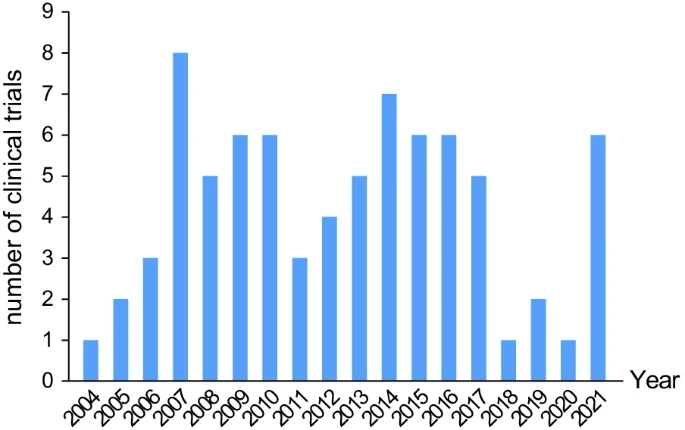
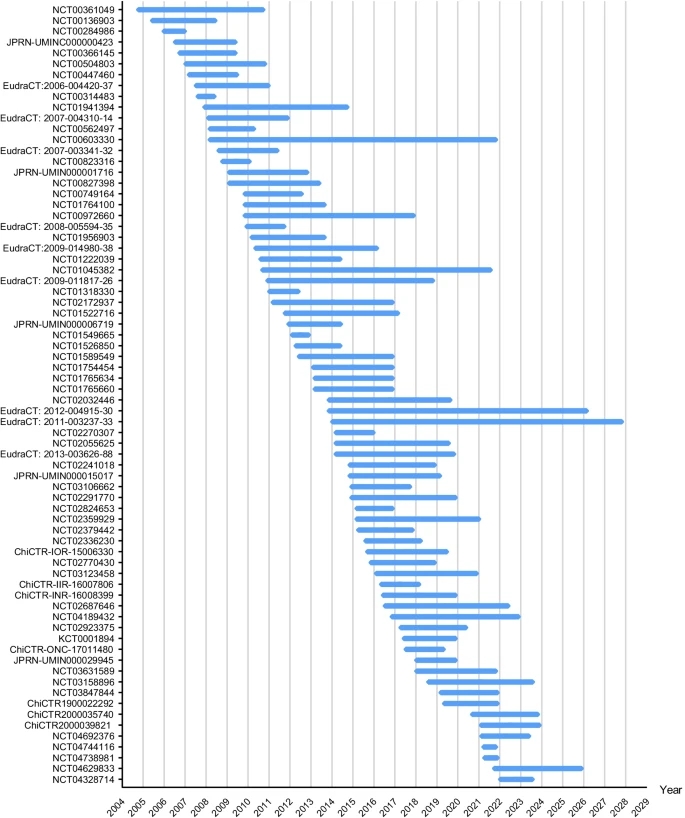
選定的涉及MSC預防或治療GVHD 的臨床試驗流程圖。其他代表伊朗臨床試驗注冊中心 (IRCT)、歐盟臨床試驗注冊中心和澳大利亞新西蘭臨床試驗注冊中心 截至2021年11月,從2004年到2021年,每年至少有一項新的涉及使用MSCs減輕移植物抗宿主病的臨床試驗注冊,其中8項研究的高峰從2007年開始。如圖3所示,MSCs的臨床試驗預防或治療移植物抗宿主病從2004年到2007年逐漸增加,從2008年到2017年保持穩定,但從2018年到2020年顯著下降,這可能是由于國際上對使用MSCs的臨床試驗的審查增加。 2018年,兩項使用MSCs的臨床試驗導致美國患者失明,導致接下來三年涉及MSCs的臨床試驗數量和針對MSCs預防或治療移植物抗宿主病的臨床試驗數量總體減少。圖4列出每個臨床試驗的開始和完成日期。臨床試驗的持續時間從9.5個月到14年不等。平均持續時間為4.19±2.70年。
每年啟動的涉及間充質干細胞預防或治療 GVHD 的臨床試驗數量 圖3
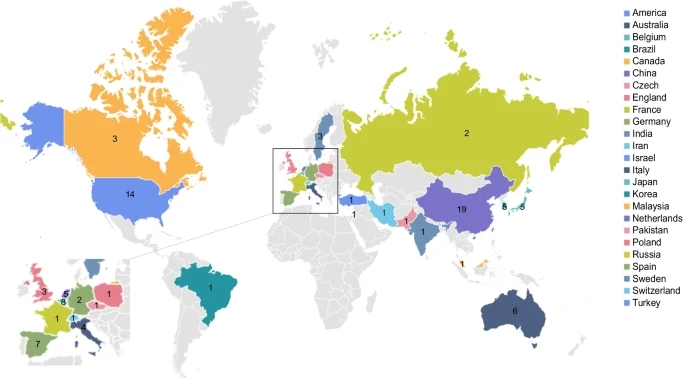
每年啟動的涉及間充質干細胞預防或治療GVHD的臨床試驗數量 圖4 臨床試驗在25個國家進行。中國舉辦的試驗數量最多,進行了19項試驗,其次是美國,舉辦了14項試驗。比利時位居第三,主辦或參與了8項試驗。這些臨床試驗覆蓋了除非洲和南極洲以外的所有大陸(圖5)。
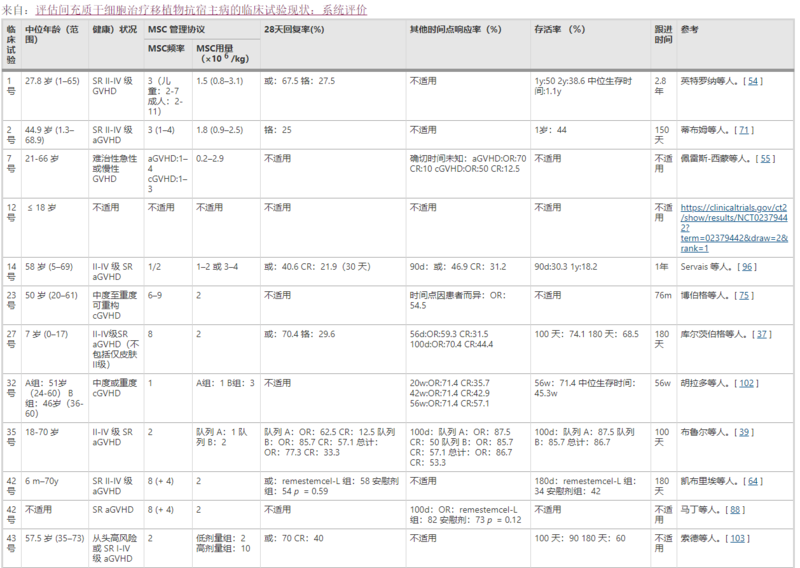
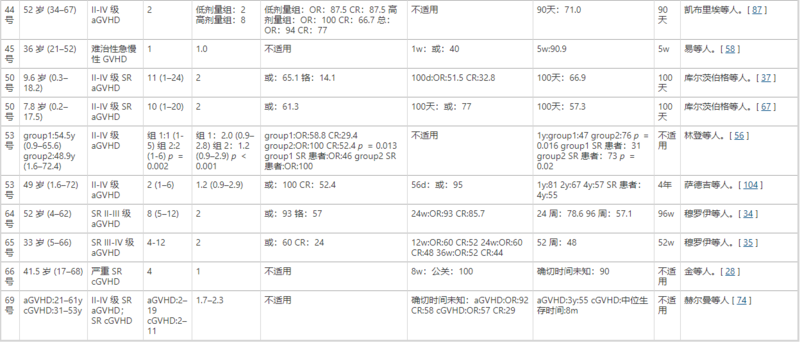
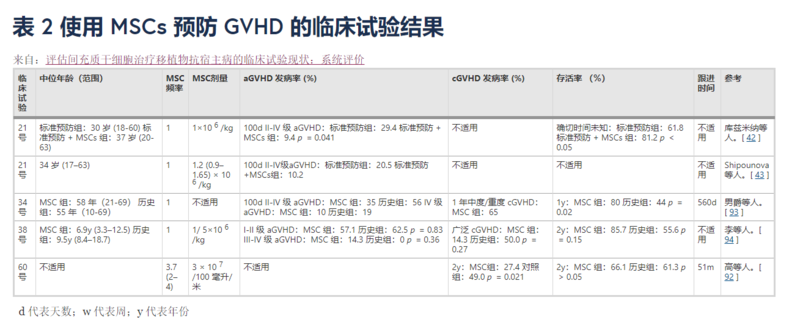
圖5 臨床試驗結果勒布朗等人報告了一例SRIV級aGvHD的9 歲男孩,他在HSCT后接受了兩次MSCs,每次輸注后癥狀明顯緩解。男孩存活了一年多。相比之下,來自同一中心的24名未接受MSCs的IV級aGvHD患者在HSCT后平均死亡2個月。 這些令人鼓舞的結果激發了人們對MSC治療GVHD的興趣,并且進行了一項多中心研究以確定MSCs是否可以改善GVHD產生了令人滿意的結果。治療了55名 SR aGvHD 患者,其中 30 名顯示完全緩解 (CR)。此外,這些CR患者的 2 年總生存率為55%。從那時起,已經進行了更多使用MSCs預防或治療 GVHD 的臨床試驗,大多數結果令人鼓舞。 如表1和表2所示,幾乎所有入組患者均患有 II-IV 級 aGVHD 或中度至重度cGVHD,并且大多數為SR。包括兒童和成人患者,年齡從2個月到72歲不等。最高28天總體緩解率(OR)達到100%(臨床試驗No.44和No.53),CR達到87.5%(試驗No.44),遠高于類固醇治療的 GVHD(OR~50%;CR, ~30%)。由于不同臨床試驗的生存觀察期限不同,很難比較總體生存率(OS),但在幾乎所有臨床試驗中,對 MSCs 有反應的患者的OS顯著高于無反應的患者。 表1MSCs治療GVHD的臨床試驗結果
表1 表2使用MSCs預防GVHD的臨床試驗結果
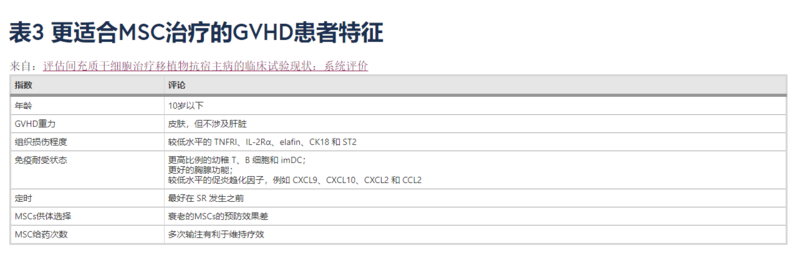
結論隨著越來越多的MSC研究顯示對GVHD小鼠模型的預防或治療效果令人滿意,涉及人類受試者的臨床試驗數量也在增加。以前的綜述總結了MSCs用于預防或治療GVHD的臨床試驗,但這些綜述中僅包含30-40項試驗。 本文納入的 79項臨床試驗中,74項為介入性試驗。因此,對這些試驗結果進行全面評估和詳細分析,可以幫助我們優化MSCs的用法和用量,找到最合適的患者群體,為未來MSCs轉化為臨床奠定基礎。我們發現最能從間充質干細胞治療中獲益的患者具有以下特點: 1、年輕患者,尤其是10歲以下的患者; 2、有皮膚但無肝臟受累的GVHD; 3、組織損傷程度較輕,表現為TNFRI、IL-2Rα、elafin、CK18、ST2水平降低; 4、更高比例的幼稚T、B細胞和imDC,更好的胸腺功能和更低水平的促炎趨化因子。此外,來自年輕供體的MSC,多次輸注MSC)。
綜上所述,隨著對間充質干細胞治療疾病特異性生物學機制的深入研究和大量臨床試驗的實踐,相信以間充質干細胞療法為基礎的治療將進一步促進臨床上GVHD的防治。 |
行業動態 干細胞治療 干細胞移植 |