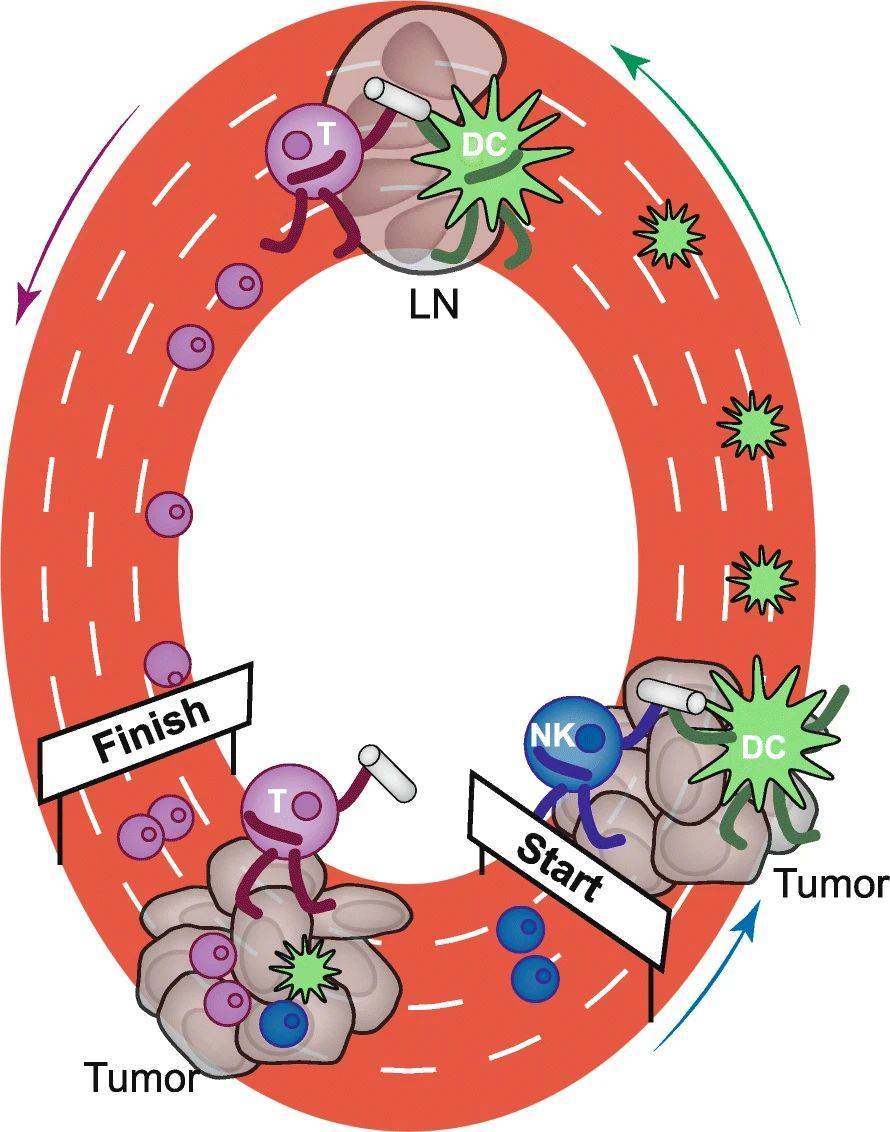
關(guān)于NK細(xì)胞療法,大家需要了解的6個(gè)真相發(fā)表時(shí)間:2022-08-25 20:40 在細(xì)胞治療領(lǐng)域,研究人員一直專注于動(dòng)員抗腫瘤T細(xì)胞。目前,F(xiàn)DA已經(jīng)批準(zhǔn)了五款CAR-T細(xì)胞療法用于血液系統(tǒng)腫瘤,應(yīng)用于實(shí)體瘤的TILs療法也在國(guó)際各大腫瘤學(xué)會(huì)議上大放異彩,有望上市。 除此之外,NK細(xì)胞作為另一種免疫細(xì)胞,也逐漸受到關(guān)注,在國(guó)際上有眾多的研究進(jìn)展。而在國(guó)內(nèi),近期一位醫(yī)生發(fā)長(zhǎng)文質(zhì)疑腫瘤醫(yī)療存在黑幕的事件在醫(yī)療圈及社會(huì)上掀起了千層浪,其中也提到NK細(xì)胞療法,成為大家關(guān)注的焦點(diǎn)。今天我們就來(lái)聊一聊究竟什么是NK細(xì)胞療法。 一,什么是NK細(xì)胞?NK細(xì)胞全名自然殺傷細(xì)胞(Natural Killer cell,NK),與T細(xì)胞等同為我們?nèi)梭w內(nèi)的核心免疫細(xì)胞。NK細(xì)胞存在于每個(gè)人的血液當(dāng)中,是免疫系統(tǒng)中的“第一反應(yīng)者”,它就像是一直在體內(nèi)執(zhí)勤的巡警,隨著血液到處跑,在“巡邏”時(shí),NK細(xì)胞不斷接觸其他細(xì)胞,一旦發(fā)現(xiàn)體內(nèi)出現(xiàn)異常細(xì)胞,馬上處理掉。它們?cè)赥細(xì)胞部署之前攻擊并在靶細(xì)胞膜上釋放含有穿孔素和顆粒酶的細(xì)胞毒性顆粒,摧毀癌細(xì)胞。 攻擊 瓦解 消滅
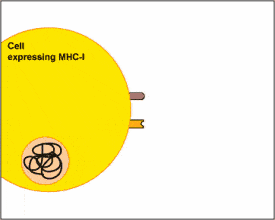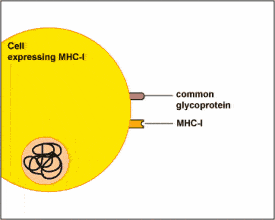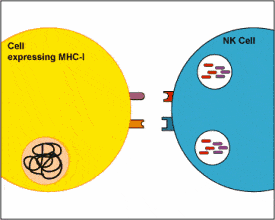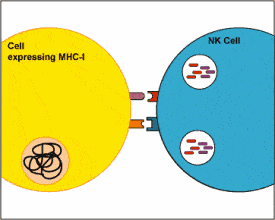
二,NK細(xì)胞的抗癌原理是什么?T細(xì)胞和NK細(xì)胞都能識(shí)別并殺死癌細(xì)胞,但它們以非常不同的方式進(jìn)行。 T細(xì)胞需要將其靶細(xì)胞的一些部分“呈現(xiàn)”給其他免疫細(xì)胞,以將它們識(shí)別為外來(lái)細(xì)胞,并使T細(xì)胞聚集成攻擊模式。 而NK細(xì)胞與T細(xì)胞不同,它們直接檢測(cè)并摧毀受感染和惡性細(xì)胞,而不必被激活或“訓(xùn)練”以對(duì)癌細(xì)胞作出反應(yīng)。然而,現(xiàn)在已經(jīng)知道NK細(xì)胞通過(guò)暴露于稱為細(xì)胞因子的免疫系統(tǒng)物質(zhì)而被激活時(shí)效果更好。 我們總結(jié)下NK細(xì)胞的三個(gè)特點(diǎn): 第一,它是人體與生俱來(lái)的免疫系統(tǒng),是走在前方的“戰(zhàn)士”,幾乎所有的腫瘤細(xì)胞都會(huì)先受到NK細(xì)胞的攻擊。 第二,免疫系統(tǒng)中的“吹哨人”,情況反饋及時(shí),一旦發(fā)現(xiàn)“敵情”,迅速“上報(bào)”并啟動(dòng)整個(gè)免疫系統(tǒng)的免疫防御和免疫殺傷功能。 第三,具有廣譜的抗腫瘤作用,不需要腫瘤特異性識(shí)別,且不會(huì)被細(xì)胞表面的主要組織相容性復(fù)合體(MHC)抑制活性限制。啟動(dòng)時(shí)間最快,而T細(xì)胞則需要經(jīng)過(guò)抗原提呈之后才能分清“敵我”。
三,NK細(xì)胞療法是什么?通俗地說(shuō),細(xì)胞免疫療法就是采集人體自身免疫細(xì)胞,經(jīng)過(guò)體外培養(yǎng),使其數(shù)量倍增,然后再回輸?shù)饺梭w,一方面用來(lái)消除癌細(xì)胞、突變細(xì)胞,另一方面激活和增強(qiáng)機(jī)體免疫力,控制癌細(xì)胞的轉(zhuǎn)移和復(fù)發(fā)。這類療法包括CAR-T、TCR-T、NK等,目前在全球被廣泛的研究。 盡管我們所有人體內(nèi)都有NK細(xì)胞,它們可以迅速進(jìn)行防御并直接攻擊腫瘤細(xì)胞,起到保護(hù)我們遠(yuǎn)離癌癥的作用。但是人體內(nèi)NK細(xì)胞數(shù)量較少,僅占白細(xì)胞的10%。并且研究發(fā)現(xiàn),人類到了25歲以后,免疫力下降,NK細(xì)胞數(shù)量變得更少,腫瘤患者及腫瘤術(shù)后患者體內(nèi)NK細(xì)胞的數(shù)量及活性都發(fā)生了一定的改變,不能非常有效地發(fā)揮抗癌作用。
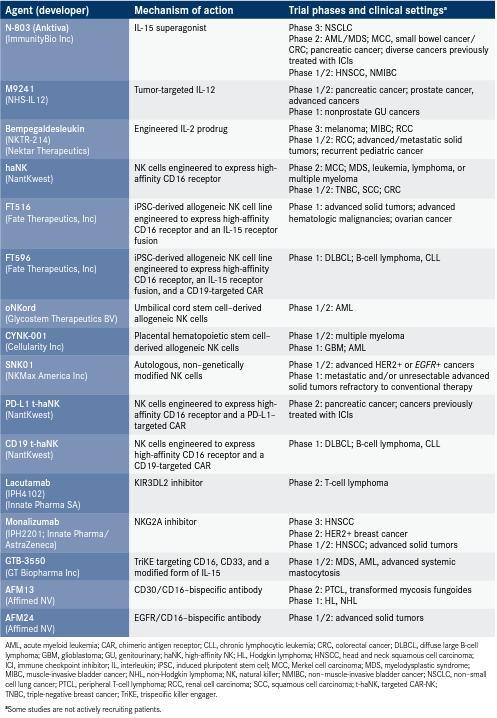
目前,國(guó)內(nèi)外的研究人員現(xiàn)在正在開(kāi)發(fā)多種方法來(lái)釋放NK細(xì)胞針對(duì)腫瘤的活性,從而提高基于NK細(xì)胞的治療的效力和特異性。 四,NK細(xì)胞療法上市了嗎?沒(méi)有。 細(xì)胞免疫療法中,目前只有CAR-T細(xì)胞療法及其產(chǎn)品較為成熟,F(xiàn)DA已經(jīng)批準(zhǔn)了五款,而NK細(xì)胞免疫療法等都還屬于研究試驗(yàn)階段。 盡管國(guó)內(nèi)外都在積極的開(kāi)展研究,但全球腫瘤醫(yī)生網(wǎng)需要提醒大家的是,目前,NK細(xì)胞免疫治療不論是中國(guó)還是美國(guó),仍然處于臨床研究階段,均未正式獲批上市進(jìn)入臨床應(yīng)用。按照規(guī)定,臨床試驗(yàn)申辦機(jī)構(gòu)不應(yīng)收取費(fèi)用。患者如有參與細(xì)胞免疫治療臨床試驗(yàn)的意愿,應(yīng)向在國(guó)家衛(wèi)生部門進(jìn)行了相關(guān)備案的醫(yī)療機(jī)構(gòu)進(jìn)行咨詢。 五,NK細(xì)胞的國(guó)際進(jìn)展有哪些?目前國(guó)際上的研究人員認(rèn)為,基于NK細(xì)胞的過(guò)繼細(xì)胞療法(ACT),包括基因修飾的嵌合抗原受體(CAR)-NK細(xì)胞,比基于T細(xì)胞的療法更安全。在臨床開(kāi)發(fā)中,基于NK細(xì)胞的治療策略還包括活化細(xì)胞因子的NK細(xì)胞,以及靶向NK細(xì)胞表面受體的抗體。 根據(jù)clinicaltrials數(shù)據(jù)庫(kù)顯示,截止4月23日,全球范圍內(nèi)NK細(xì)胞免疫療法相關(guān)的臨床試驗(yàn)有225例正在進(jìn)展中,且大部分都是由醫(yī)院或者學(xué)術(shù)機(jī)構(gòu)自主開(kāi)展的學(xué)術(shù)研究;應(yīng)用到癌癥治療領(lǐng)域的研究,有174例臨床試驗(yàn)在進(jìn)展。
國(guó)際上用于腫瘤免疫治療的NK細(xì)胞策略主要有以下類。 01 體外活化的自體或異體NK細(xì)胞方法 目前國(guó)內(nèi)和國(guó)際上專注于研發(fā)“過(guò)繼性”NK細(xì)胞療法,就是從密切相關(guān)的供體收集NK細(xì)胞并在體外擴(kuò)增將其注入患者體內(nèi)。 02 聯(lián)合NK細(xì)胞和單抗藥(如免疫檢查點(diǎn)抑制劑)來(lái)誘導(dǎo)抗體特異的細(xì)胞毒性 檢查點(diǎn)治療與其他NK指導(dǎo)的免疫治療相結(jié)合,可以針對(duì)目前對(duì)現(xiàn)有療法無(wú)反應(yīng)的多種類型的腫瘤。 盡管NK細(xì)胞對(duì)抗腫瘤的殺傷機(jī)制是非特異性的,并不依賴于腫瘤相關(guān)抗原的識(shí)別,但同樣存在免疫檢查點(diǎn)的激活或抑制機(jī)制。腫瘤細(xì)胞可以表達(dá)的針對(duì)NK細(xì)胞免疫檢查點(diǎn)的配體,能夠抑制NK細(xì)胞介導(dǎo)的腫瘤細(xì)胞裂解,因此,以限制這種抑制作用,目前開(kāi)發(fā)一系列針對(duì)腫瘤-NK細(xì)胞的抑制型免疫檢查點(diǎn)的抗體。 如抗EGFR的西妥昔單抗,西妥昔單抗可以激活NK細(xì)胞的ADCC 效應(yīng),并啟動(dòng)NK細(xì)胞的適應(yīng)性免疫應(yīng)答。 另外,研究發(fā)現(xiàn)NK細(xì)胞中的PD-1在幾種癌癥中高表達(dá),包括頭頸癌,甲狀腺癌,霍奇金淋巴瘤(HL),消化道癌(食道癌,肝癌,大腸癌,胃癌和膽道癌),乳腺癌,卡波濟(jì)肉瘤,腎細(xì)胞癌和多發(fā)性骨髓瘤。最近的研究表明,當(dāng)PD-L1陰性的腫瘤對(duì)抗PD-L1治療有反應(yīng)時(shí),這種作用可能是由PD-L1+NK細(xì)胞介導(dǎo)的。PD-L1+用抗PD-L1處理的NK細(xì)胞顯示出增強(qiáng)的激活和效應(yīng)子功能。 03 構(gòu)建CAR-NK細(xì)胞免疫療法 嵌合抗原受體改造的NK細(xì)胞:能顯著提高NK細(xì)胞療效特異性。這個(gè)思路和CAR-T的構(gòu)建類似:CAR包括胞外的識(shí)別結(jié)構(gòu)域(如scFv)識(shí)別腫瘤特異性抗原;一個(gè)跨膜結(jié)構(gòu)域,和一個(gè)胞內(nèi)信號(hào)結(jié)構(gòu)域(CD3ζ 鏈)可以誘導(dǎo)NK細(xì)胞的活化。 根據(jù)德克薩斯大學(xué)安德森分校癌癥中心 I / IIa期試驗(yàn)的結(jié)果,以CD19為靶點(diǎn)的臍血來(lái)源的嵌合抗原受體(CAR)自然殺傷(NK)細(xì)胞療法治療使患有復(fù)發(fā)性或難治性非霍奇金淋巴瘤(NHL)和慢性淋巴細(xì)胞性白血病(CLL)的患者出現(xiàn)臨床緩解,并且沒(méi)有重大毒性反應(yīng)。該試驗(yàn)結(jié)果發(fā)表在《新英格蘭醫(yī)學(xué)雜志》上。 在參與該研究的11位患者中,有8位(73%)對(duì)治療有反應(yīng),其中7位完全緩解,這意味著他們?cè)谥形浑S訪13.8個(gè)月時(shí)無(wú)疾病跡象。 輸注后1個(gè)月內(nèi)對(duì)CD19 CAR NK細(xì)胞療法的反應(yīng)明顯,并且在輸注后1年內(nèi)確認(rèn)了這項(xiàng)治療的持久性。
這是一種新型的療法,首先需要從臍帶血庫(kù)中存儲(chǔ)的臍帶血中分離出NK細(xì)胞,并對(duì)它們進(jìn)行基因工程改造,引入可識(shí)別癌細(xì)胞表面靶標(biāo)的CAR。這些CAR NK細(xì)胞回輸給患者。 與CAR-T療法相比,其最大的優(yōu)勢(shì)在于不會(huì)引起移植物抗宿主病(GVHD),這是一種在CAR-T療法中常見(jiàn)的由供體T細(xì)胞攻擊受體中的健康細(xì)胞引起的破壞性疾病。由于NK細(xì)胞不會(huì)引起GVHD,因此可以將它們從供體提供給接受者,而無(wú)需進(jìn)行匹配。這意味著您可以從一個(gè)供體中制備多個(gè)劑量的CAR NK細(xì)胞來(lái)治療多個(gè)患者。 從診斷到癌癥治療的時(shí)間大大縮短。 04 AFM13聯(lián)合cbNK細(xì)胞治療 在2021年AACR會(huì)議上,由全球知名的美國(guó)MD安德森癌癥中心公布的一項(xiàng)臍血來(lái)源的自然殺傷(cbNK)細(xì)胞聯(lián)合先天細(xì)胞接合劑(ICE?)AFM13(CD16A / CD30)治療淋巴瘤的初步臨床試驗(yàn)結(jié)果: 所有四名患者均出現(xiàn)強(qiáng)烈響應(yīng),病灶顯著縮小,其中包含兩名完全緩解和兩名部分緩解,總體客觀緩解率為100%; 沒(méi)有觀察到細(xì)胞因子釋放綜合征,神經(jīng)毒性綜合征或移植物抗宿主病的事件; 這項(xiàng)NK細(xì)胞研究目前正在招募第二批患者。 研究人員說(shuō),“這項(xiàng)開(kāi)創(chuàng)性的首次人體研究為我們提供了初步的安全性和有效性數(shù)據(jù)。這些初步結(jié)果表明,AFM13可能具有幫助NK細(xì)胞靶向和破壞癌細(xì)胞的潛力,為治療各種血液學(xué)和實(shí)體瘤提供選擇。在我們?nèi)虢M的前四名患者中,客觀緩解率達(dá)到100%的結(jié)果令人印象深刻。 AFM13是一種的先天性細(xì)胞接合劑(ICE?),可激活自身免疫系統(tǒng)來(lái)攻擊CD30陽(yáng)性的血液系統(tǒng)腫瘤。AFM13通過(guò)激活自然殺傷(NK)細(xì)胞和巨噬細(xì)胞,讓免疫細(xì)胞釋放穿孔素,在腫瘤細(xì)胞膜上形成孔,粒酶通過(guò)該孔進(jìn)入腫瘤細(xì)胞,觸發(fā)CD30陽(yáng)性腫瘤細(xì)胞的特異性和選擇性殺傷。 05 NK細(xì)胞激活細(xì)胞因子 FDA即將批準(zhǔn)一款NK細(xì)胞激活細(xì)胞因子,白介素15(IL-15)超激動(dòng)劑N-803(Anktiva;以前為ALT-803),目前開(kāi)發(fā)該療法的公司ImmunityBio預(yù)計(jì)將在2021年向FDA批準(zhǔn)N-803聯(lián)合BCG疫苗的生物制劑許可申請(qǐng),以治療非肌肉浸潤(rùn)性膀胱癌(NMIBC)患者。 06如何正確看待NK細(xì)胞療法?由于全球面對(duì)癌癥這個(gè)世界公敵仍然需要更多有效的治療手段,因此,包括NK已及其他細(xì)胞免疫療法,都是科學(xué)家們?yōu)榱藨?zhàn)勝癌癥這個(gè)終極目的而不斷研發(fā)的新興療法。 癌癥治療從來(lái)都不是一種療法就能大功告成的,需要多種治療手段的聯(lián)合治療,手術(shù)、放療和化療的三大中流砥柱地位無(wú)人能撼動(dòng),但是這三大傳統(tǒng)療法還未滿足治療需求。因此,靶向藥、免疫治療和細(xì)胞治療接連問(wèn)世,來(lái)彌補(bǔ)傳統(tǒng)療法的不足。通過(guò)修復(fù)腫瘤患者的免疫功能、提高其抗腫瘤能力將代表腫瘤治療的發(fā)展方向。癌癥免疫治療、細(xì)胞免疫治療的地位不容忽視。 北京大學(xué)腫瘤醫(yī)院的朱軍教授說(shuō)道:從腫瘤專科醫(yī)生的角度,我認(rèn)為細(xì)胞免疫療法雖然不能全面替代癌癥臨床治療中別的療法,但它有它的作用,有它的幫助,也應(yīng)該有它的一席之地,不能一棍子打死。而且在細(xì)胞免疫治療領(lǐng)域的研究上,我們并不比美國(guó)做得晚,做得少。但是,我們有我們的軟肋,就是缺乏合理的管理和審批以及監(jiān)控監(jiān)管,導(dǎo)致細(xì)胞免疫治療研究長(zhǎng)期游走在灰色地帶。對(duì)于患者和臨床醫(yī)生而言,只有在嚴(yán)格監(jiān)管下的免疫細(xì)胞療法以及產(chǎn)品才能保障臨床的安全和有效。” 因此,對(duì)于這類新技術(shù)大家應(yīng)該理性對(duì)待。也希望相關(guān)部門能盡快規(guī)范新興療法的審批管理和監(jiān)控監(jiān)管,讓對(duì)患者有益的醫(yī)療手段能夠早日正規(guī)實(shí)施。 本文轉(zhuǎn)自全球腫瘤醫(yī)生網(wǎng) 參考資料: https://www.mdanderson.org/newsroom/cd19-car-nk-cell-therapy-achieves-73-percent-response-rate-in-patients-with-leukemia-and-lymphoma.h00-159379578.html https://nantkwest.wpengine.com/immunitybio-announces-primary-endpoint-met-of-phase-2-3-trial-for-bcg-unresponsive-non-muscle-invasive-bladder-cancer-cis-with-72-complete-response-rate/ https://www.affimed.com/affimed-highlights-the-potential-of-its-innate-cell-engager-afm24-as-egfr-targeting-therapy-for-solid-tumors-as-monotherapy-and-in-combination-with-adoptive-nk-cell-transfer-at-aacr-virtual-annual-mee/ https://www.affimed.com/affimed-announces-presentation-at-aacr-highlighting-initial-data-from-phase-1-study-of-cord-blood-derived-natural-killer-cells-pre-complexed-with-innate-cell-engager-afm13/ |
行業(yè)動(dòng)態(tài) 干細(xì)胞治療 干細(xì)胞移植 |